
当研究室では、有機合成を基盤に研究を進めており、体内のタンパク質に作用する化合物を有機合成し、細胞レベルおよび動物レベルでの生物活性評価を行うことで、医薬品の候補となる化合物を探索しています。また、体内の各種酵素に対して安定性を持つ化合物を創出することで、新規の機能性材料への応用も目指しています。以下に主な研究内容を示します。
1. ニューロンへの分化を誘導する新規ビタミンK誘導体の探索
ビタミンKには植物由来のビタミンK1(1)と菌類由来のビタミンK2(2)が存在し、生体内で血液凝固因子や骨形成に関与する補酵素として働くことが一般的に知られています。近年、ビタミンKは核内受容体を介した転写調節作用など、生体内で重要な役割を担っていることが明らかにされつつあります。また、特にビタミンKは脳に多く存在するため、脳において未解明の重要な機能を担っている可能性が考えられています。その一例として、ビタミンKがマウス胎仔大脳由来の脳神経幹細胞をニューロンへ選択的に分化させる作用を持つことが最近の私たちの研究で示されました。私たちは、このビタミンKの骨格を基に、分化誘導作用をさらに高めた誘導体のデザイン・合成を行い、強力な作用を持つ化合物を探索しています。脳神経幹細胞は成人の脳にも存在することが近年の研究で確認されており、ニューロンへの分化を強力に誘導する化合物は、アルツハイマー病など脳神経変性疾患で失われたニューロンを再生する可能性があります(図1)。
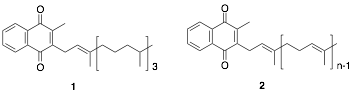
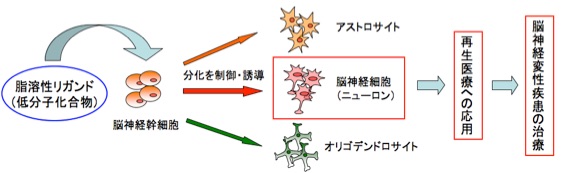
図1. 神経分化誘導作用をもつビタミンK誘導体の創製
2. 抗ウイルス作用を持つビタミンK誘導体の探索
鹿児島大学医学部との共同研究により、当研究室で合成したビタミンK誘導体の化合物ライブラリーに、新型コロナウイルス (SARS-CoV-2) の増殖を抑制する作用がある化合物が含まれていることが明らかになりました。また、その作用機序として、ビタミンK3およびビタミンK2誘導体がウイルスの増殖に必須の酵素である3CLプロテアーゼおよびRNA依存性RNAポリメラーゼを阻害し、ウイルスの複製を停止させることが判明しました(図2)。そこで、これらの作用をさらに強化することを目的に、ビタミンK3とビタミンK2の化学構造を修飾した化合物を合成し、より強い作用を持つ化合物を探索しています。
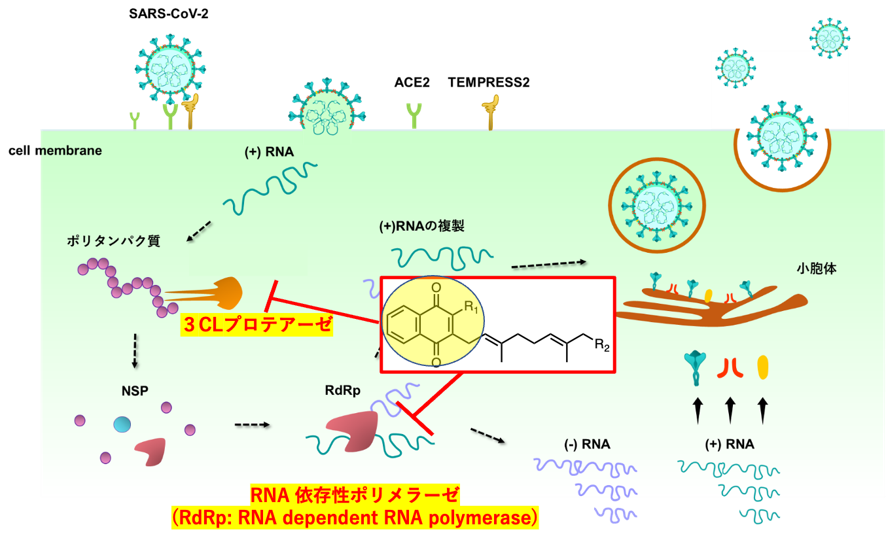
図2. ウイルスが増殖するための必須の酵素を阻害するビタミンK誘導体の探索
3. 肝がん細胞に対して増殖抑制作用を示す非環式レチノイド誘導
肝細胞がんは、アルコール摂取やC型/B型肝炎ウイルス(HCV/HBV)、生活習慣などのさまざまな要因により発症する疾患です。治療水準が向上した現代においても再発率が高く、5年後および10年後の生存率が低いため、新たな治療薬が求められています。そこで私たちは、従来の抗がん剤と同様に肝細胞がんの増殖抑制作用を持つ非環式レチノイド(ACR:acyclic retinoid)に着目しました。ACRは肝細胞がんの増殖抑制作用を有するだけでなく、特有の作用として肝細胞がんの再発抑制作用を持つことが報告されています。そこで、ACRの側鎖構造を化学修飾することにより、作用を強化した新規ACR誘導体の創製を目指しています(図3)。
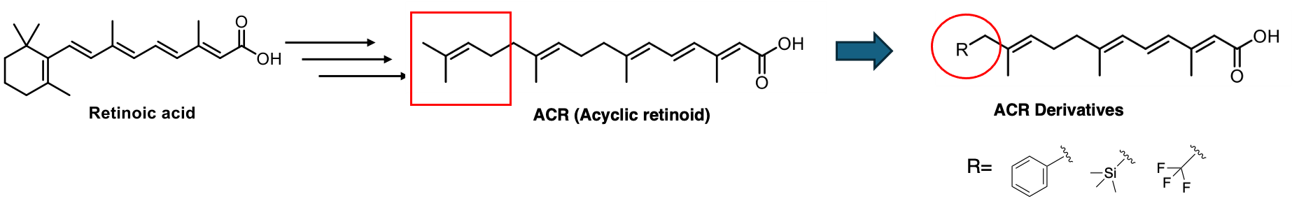
図3.肝がん細胞の増殖を抑制する非環式レチノイド誘導体の合成
4. 体内で安定に存在できるコラーゲンペプチドの合成
コラーゲンは腱、軟骨、骨の有機間質、そして眼の角膜のような結合組織中に見られる重要なタンパク質であり、人工臓器をはじめとした再生医療へ応用するための材料として注目されています。また、左巻きのポリペプチド鎖が寄り集まって右巻きの3本鎖ヘリックス構造をとることで、繊維組織や骨格の構造維持に必要な性質を示すことが知られており、化学的にも興味深い物質です(図4)。当研究室では体内の加水分解酵素に対して耐性をもつ安定な人工コラーゲンの創製を行っています。つまり、コラーゲンを構成するα−アミノ酸を他の化合物に変換したコラーゲンペプチド模倣物の合成を行い、新規の機能性材料への応用を目指しています。
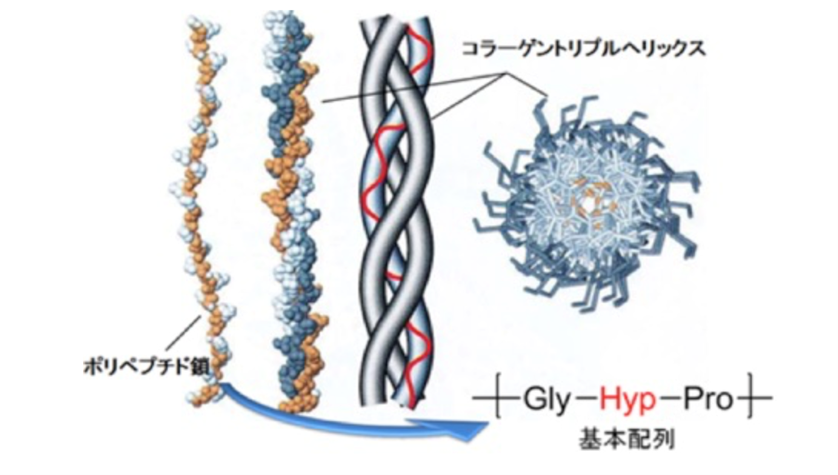
図4. コラーゲンの基本構造
5. 新規糖質類縁体の合成化学的構築と生理活性物質への応用
天然由来の糖化合物は、複雑な水酸基の選択的保護やグリコシル化反応などのため合成が困難なうえ、生体内の酵素により速やかに分解されてしまう欠点を持っています。そこで全く新しい糖質類縁体によりそれらの問題を解決する一助にする目的で、C-グリコシドである“糖アミノ酸(GA:glycamino acid)”を構築単位とする新規糖質類縁体を合成しています。このGAはC-1位にカルボキシル基を有し、水酸基の一つを選択的にアミノ基に置換した単糖誘導体です。GAをビルディングブロックとしてアミド結合を有するオリゴ糖類縁体を容易に構築出来ると同時に、結合配位をGA単位で完全に制御出来る利点があります。またこのように合成した糖アミノ酸は、天然の糖鎖と比較してどのような生物活性を有するのかを調べています。さらに、これらの化合物の中にはβ-アミノ酸とみなすことが出来るものがあり、引き続き機能性材料としての可能性を検討しています。
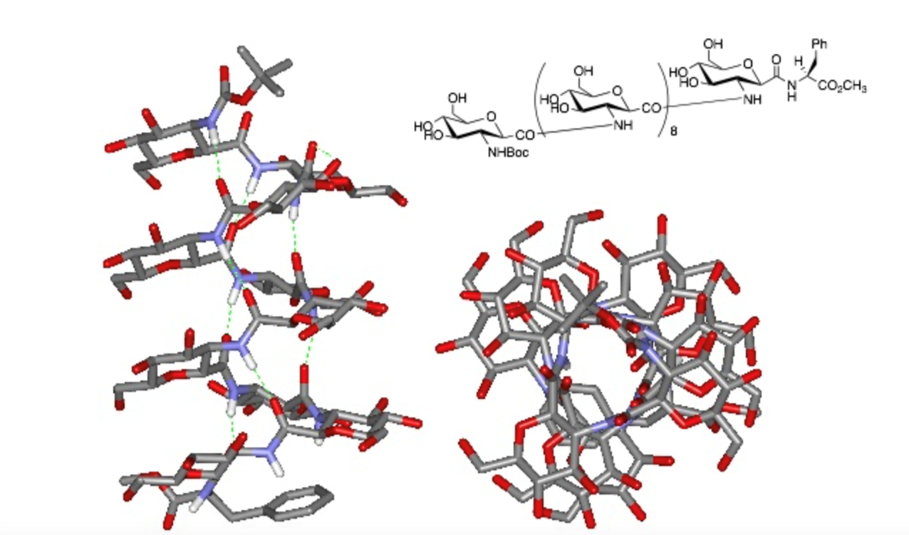
図5. 糖アミノ酸の立体構造
6. 核内受容体に対してアゴニスト活性をもつ新規化合物の探索
脂溶性ビタミンはビタミンA、D、Kなどが存在し、それらは核内受容体であるレチノイドX受容体(RXR: retinoid X receptor)、ビタミンD受容体(VDR: vitamin D receptor)、ステロイドX受容体(SXR: steroid X receptor)にそれぞれ特異的に結合し、各種遺伝子の発現を誘導することが知られています。私たちはこれまでに、それら脂溶性ビタミン類の構造の一部を他の官能基に変換するなどして受容体との結合能を高め、高い生理活性を有する化合物を得ることに成功してきました。その一例として、ビタミンK2(メナキノン−3)の側鎖末端部分にベンゼン環を導入した化合物を合成し(図6)、SXRを介した転写活性を調べたところ、SXRリガンドとして知られているリファンピシンより強い活性を示すことが明らかとなりました。その結合状態を計算科学の手法を用いて、化合物が受容体にどのように結合しているのかを解析しました。これらの情報を基にして、さらに強いアゴニスト活性を有する化合物を見出す試みを行っています。
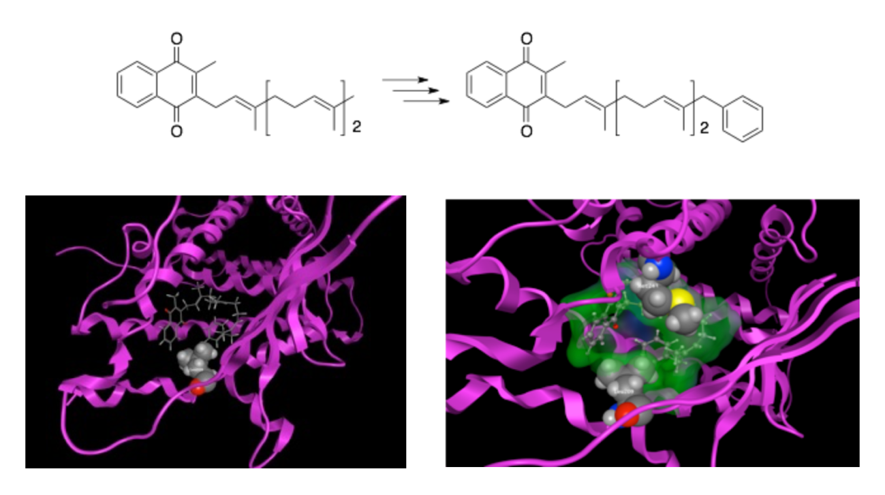
図6. SXRとリガンドとのドッキングシミュレーション
